العلاج الضوئي المناعي: الجراحة اليابانية بالضوء لعلاج السرطان المتقدم
للمرضى والعائلات: دليلك للعلاج الضوئي المناعي
ما هو العلاج الضوئي المناعي بلغة بسيطة؟
تخيل علاجاً يعمل بهذه الطريقة:
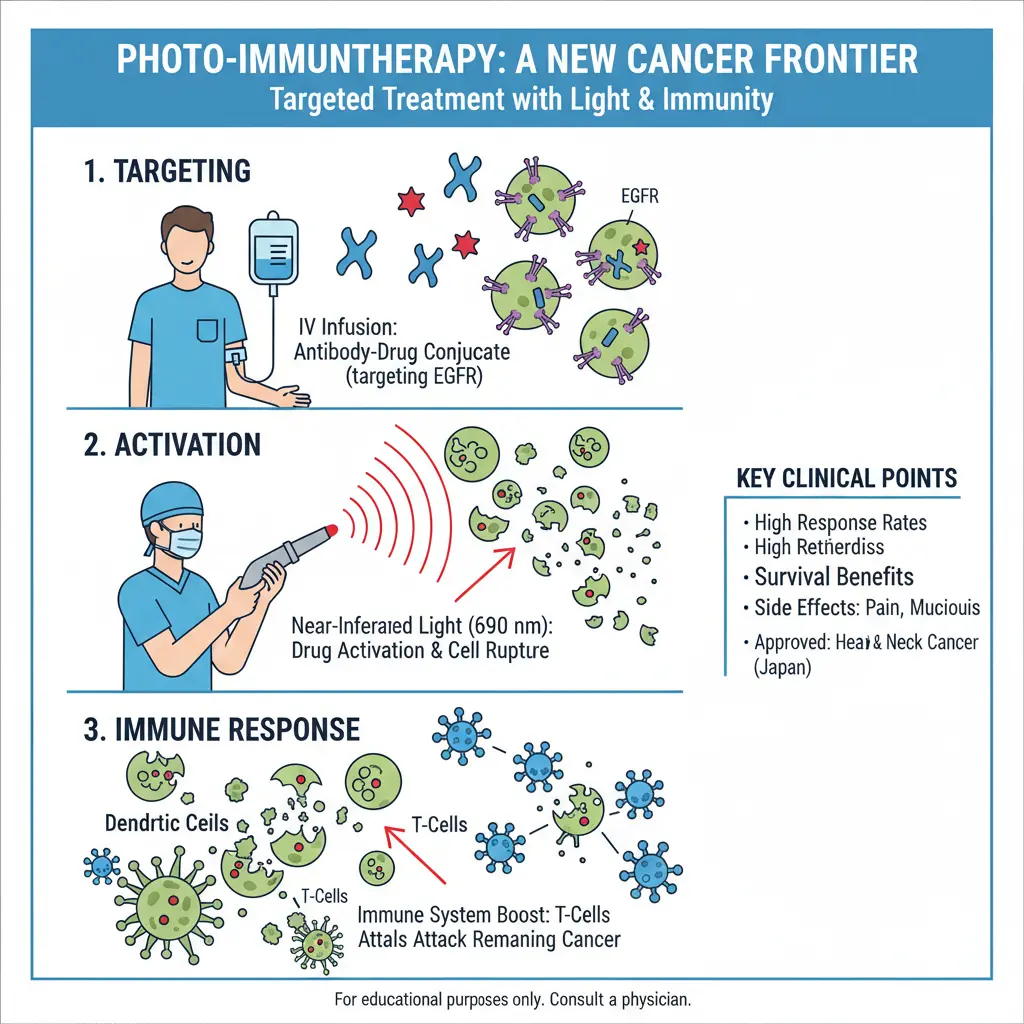
- الخطوة 1: تتلقى حقنة وريدية من دواء "ذكي" يبحث ويلتصق فقط بخلاياك السرطانية - مثل جهاز تتبع GPS مرتبط بهدف محدد.
- الخطوة 2: بعد حوالي يوم، يسلط الجراح ضوء ليزر أحمر خاص مباشرة على الورم.
- الخطوة 3: ينشط الضوء الدواء، مما يتسبب في انتفاخ الخلايا السرطانية وانفجارها - حرفياً في غضون دقائق. وهنا الجزء الرائع: عندما تموت هذه الخلايا السرطانية، ترسل إشارات توقظ جهازك المناعي لمهاجمة أي خلايا سرطانية متبقية في جميع أنحاء جسمك.
هذا ليس خيالاً علمياً. إنه العلاج الضوئي المناعي بالأشعة تحت الحمراء القريبة (NIR-PIT)، وهو متاح في اليابان منذ عام 2021 للمرضى المصابين بسرطان الرأس والرقبة غير القابل للجراحة.
لمن هذا العلاج؟
العلاج الضوئي المناعي معتمد حالياً في اليابان للمرضى الذين يعانون من:
- سرطان الرأس والرقبة الموضعي المتقدم أو المتكرر الذي لا يمكن استئصاله جراحياً
- الأورام التي تعبر عن EGFR (بروتين على سطح الخلايا السرطانية) - يلزم إجراء اختبار قبل العلاج
- المرضى الذين جربوا بالفعل العلاجات القياسية مثل العلاج الكيميائي أو الإشعاعي أو كليهما
عادةً لا يكون مناسباً لـ:
- المرضى الذين يعانون من نقائل بعيدة واسعة الانتشار (على الرغم من أن الأبحاث تستكشف هذا)
- من لا يمكنهم الخضوع للتخدير العام بأمان
- المرضى الذين تظهر أورامهم تعبيراً منخفضاً أو معدوماً لـ EGFR
- الأشخاص الذين لا يستطيعون الوصول إلى مركز علاج متخصص مجهز بنظام الليزر
ماذا يحدث بالضبط في يوم العلاج؟
اليوم الأول (يوم الحقن): تصل إلى المستشفى وتتلقى مركب الجسم المضاد-الدواء (سيتوكسيماب ساروتالوكان، الاسم التجاري أكالوكس®) عبر الوريد. تستغرق عملية الحقن حوالي ساعة. ثم تعود إلى المنزل أو تبقى في المستشفى بينما ينتشر الدواء في جسمك ويلتصق بخلاياك السرطانية خلال 20-28 ساعة القادمة.
اليوم الثاني (يوم العلاج): يتم نقلك إلى غرفة العمليات ووضعك تحت التخدير العام. يضع الجراح ألياف الليزر لتوصيل الضوء الأحمر (بطول موجي 690 نانومتر) بدقة إلى الورم. يستمر التعرض للضوء عادة من دقائق إلى ساعات اعتماداً على حجم الورم وموقعه. بعد ذلك، تتم مراقبتك عن كثب أثناء استيقاظك من التخدير.
الأيام والأسابيع التالية: يعاني معظم المرضى من بعض الألم والتورم في المنطقة المعالجة - وهذا متوقع ويتم التعامل معه بالأدوية. قد تحتاج إلى دعم تغذية مؤقت إذا كان الورم في الفم أو الحلق. سيحدد فريقك الطبي مواعيد للتصوير المتابع (عادةً الأشعة المقطعية أو PET) بعد حوالي 4-8 أسابيع لتقييم الاستجابة.
أسئلة شائعة يطرحها المرضى
هل هذا مؤلم؟
أثناء العملية، أنت تحت التخدير، لذا لا تشعر بأي شيء. بعد ذلك، الألم في موقع العلاج شائع جداً - تم الإبلاغ عنه في أكثر من 90٪ من المرضى - لكن يتم التعامل معه عادة بفعالية باستخدام مسكنات الألم القياسية.
هل سيترك ندبة؟
على عكس الجراحة التقليدية، لا يوجد شق جراحي. ومع ذلك، إذا كان الورم قريباً من سطح الجلد، فقد تكون هناك بعض التغيرات الجلدية الموضعية. داخلياً، ستلتئم المنطقة المعالجة مثل أي جرح آخر.
كم عدد جلسات العلاج التي يمكنني الحصول عليها؟
يتلقى بعض المرضى جلسات متعددة. يعتمد القرار على استجابتك، وصحتك العامة، وما إذا ظهرت آفات جديدة في مواقع يمكن الوصول إليها.
هل يمكن أن يساعد هذا إذا انتشر سرطاني إلى أجزاء أخرى من الجسم؟
العلاج نفسه موضعي - فهو يؤثر فقط على المناطق المعرضة للضوء. ومع ذلك، لأنه يحفز استجابة مناعية، هناك احتمالية لحدوث "تأثيرات بعيدة" حيث يهاجم الجهاز المناعي الأورام البعيدة. هذا مجال بحث نشط، وتختلف النتائج من مريض لآخر.
للأطباء: نظرة عملية
الاستطباب الحالي
العلاج الضوئي المناعي بالأشعة تحت الحمراء القريبة (NIR-PIT) باستخدام سيتوكسيماب ساروتالوكان (أكالوكس®) معتمد في اليابان للمرضى الذين يعانون من سرطان الخلايا الحرشفية في الرأس والرقبة الموضعي المتقدم أو المتكرر غير القابل للجراحة والذي يعبر عن EGFR، بعد فشل العلاجات القياسية.
البيانات السريرية الرئيسية (النتائج الواقعية)
خطوات الإجراء
- اختيار المريض: التأكد من عدم قابلية الورم للجراحة، إيجابية EGFR (باستخدام الكيمياء الهيستولوجية المناعية)، حالة أداء مناسبة، وسلامة المجرى الهوائي.
- الحقن: إعطاء سيتوكسيماب ساروتالوكان وريدياً (الجرعة القياسية: 640 مغ/م²).
- التنشيط بالضوء: بعد 20-28 ساعة من الحقن، تحت التخدير العام، تسليط ضوء ليزر بطول موجي 690 نانومتر بكثافة 50-150 جول/سم² (تعتمد الجرعة على عمق الورم وموقعه).
- المراقبة بعد الإجراء: مراقبة الألم، الوذمة، سلامة المجرى الهوائي، النزيف، وتكون الناسور. غالباً ما يكون الدعم متعدد التخصصات (إدارة الألم، التغذية، حماية المجرى الهوائي) ضرورياً.
الأحداث الضائرة (بيانات واقعية)
| الحدث الضائر | نسبة الحدوث | الدرجة ≥3 |
|---|---|---|
| الألم | 92.5% | 17.5% |
| التهاب الغشاء المخاطي/الفم | 80.0% | 17% |
| وذمة الحنجرة | ~67% | 8% |
| عسر البلع | ~50% | غير محدد |
| النزيف | ~50% | غير محدد |
| الناسور | ~33% | غير محدد |
غالباً ما تكون الإدارة الاستباقية للمجرى الهوائي (بما في ذلك فتح القصبة الهوائية الوقائي في حالات مختارة) والتغذية المعوية المؤقتة ضرورية.
اعتبارات اختيار المرضى
- أقوى مؤشر للاستجابة: مستوى تعبير EGFR (الارتفاع في التعبير يرتبط بنتائج أفضل)
- موانع الاستعمال: عدم القدرة على تحمل التخدير العام، اعتلال تخثر شديد غير قابل للتصحيح، غزو الورم للأوعية الدموية الكبرى حيث يكون توصيل الضوء مستحيلاً
- اعتبارات نسبية: العلاج الإشعاعي السابق لنفس الموقع ليس مانعاً؛ العديد من المرضى المعالجين تلقوا علاجاً إشعاعياً سابقاً
العلوم بلغة واضحة: كيف يعمل العلاج الضوئي المناعي
الآلية: ضربة مزدوجة
الضربة 1: التدمير الفيزيائي
يرتبط الدواء (سيتوكسيماب-IR700) بـ EGFR على الخلايا السرطانية. عند التعرض لضوء الأشعة تحت الحمراء القريبة بطول 690 نانومتر، تخضع الصبغة لتغيير هيكلي يجعلها كارهة للماء. هذا يتسبب في تجمع مركبات الجسم المضاد-الصبغة وتشويه غشاء الخلية فيزيائياً - مما يؤدي إلى انتفاخ وتمزق سريع. يحدث هذا في غضون دقائق، بشكل مستقل عن الأكسجين، مما يجعله فعالاً حتى في بيئات الورم منخفضة الأكسجين.
الضربة 2: موت الخلايا المناعي (ICD)
عندما تنفجر الخلايا السرطانية، تطلق أنماطاً جزيئية مرتبطة بالضرر (DAMPs) ومستضدات ورمية. هذه "إشارة الخطر" تجذب الخلايا المتغصنة، التي تقدم المستضدات إلى الخلايا التائية، محولة الورم بشكل فعال إلى لقاح موضعي. النتيجة هي استجابة مناعية جهازية يمكنها مهاجمة النقائل التي لم تتعرض للضوء.
آخر الأبحاث (2025-2026)
ما بعد سرطان الرأس والرقبة
بينما المعتمد حالياً فقط لسرطان الخلايا الحرشفية في الرأس والرقبة، تتوسع الأبحاث بسرعة:
| نوع السرطان | الهدف | الحالة |
|---|---|---|
| سرطان الثدي (الثلاثي السلبي) | ICAM-1 | ما قبل السريري - فعال في نماذج الفئران |
| سرطان المثانة (غير الغازي للعضلات) | EGFR, Nectin-4, TROP-2 | ما قبل السريري - قتل خلوي قوي |
| سرطان البنكرياس | استهداف السدى | ما قبل السريري - يعيد تشكيل البيئة الدقيقة للورم |
| سرطان المبيض | EGFR, Her2, FOLR1, TROP-2, TF | ما قبل السريري - تأكيد تحفيز ICD |
| الورم الأرومي العصبي (الأطفال) | GD2 | ما قبل السريري - كبت ورم كبير |
استراتيجيات الدمج قيد التطوير
- PIT الموجه لـ CD25 + IL-15 + مضاد PD-1: يستنزف الخلايا التائية التنظيمية في البيئة الدقيقة للورم، مما يعزز نشاط الخلايا التائية CD8+. في نماذج الفئران، حقق هذا المزيج استجابات كاملة بنسبة 90%.
- PIT الموجه لـ FAP لتوصيل الدواء: بتدمير الأرومة الليفية المرتبطة بالسرطان، يقلل هذا النهج الحاجز المادي أمام اختراق العلاج الكيميائي.
- مزيج ناهض STING: تنشيط مسار المناعة الفطرية يتآزر مع ICD المستحث بـ PIT لمناعة أقوى مضادة للورم.
القيود والأسئلة غير المجابة
- معظم البيانات تأتي من بلد واحد (اليابان) بنظام رعاية صحية محدد
- أعداد المرضى في الدراسات المنشورة لا تزال صغيرة نسبياً (عشرات إلى مئات قليلة)
- النتائج طويلة المدى لما بعد 2-3 سنوات لا تزال قيد الجمع
- يتطلب العلاج معدات متخصصة وفرقاً متعددة التخصصات، مما يحد من إمكانية الوصول
- لا يستجيب جميع المرضى - مستوى تعبير EGFR حاسم، وحتى بعض الأورام الإيجابية لـ EGFR تظهر مقاومة
- العدد الأمثل لجلسات العلاج وفترات إعادة العلاج لا تزال قيد التحديد
كيف تتحدث مع طبيبك عن العلاج الضوئي المناعي
إذا كنت أنت أو أحد أحبائك مصاباً بسرطان الرأس والرقبة المتقدم ولم تعد العلاجات القياسية فعالة، إليك أسئلة لتوجيه محادثة مثمرة مع طبيب الأورام:
- "هل تم اختبار ورمي لتعبير EGFR؟ إذا لم يكن كذلك، هل يمكننا اختباره؟" (هذا ضروري - العلاج يعمل فقط إذا كان سرطانك يحتوي على كمية كافية من EGFR.)
- "بناءً على حالتي - موقع الورم، العلاجات السابقة، والصحة العامة - هل تعتقد أنني قد أكون مرشحاً للعلاج الضوئي المناعي؟"
- "هل لديك أي خبرة مع هذا العلاج، أو هل تعرف زملاء أو مراكز لديها هذه الخبرة؟" (حتى لو كان طبيبك لا يستطيع تقديمه، قد يعرف طرق الإحالة أو التجارب السريرية.)
- "هل هناك أي تجارب سريرية في الولايات المتحدة أو أوروبا أو اليابان قد أكون مؤهلاً لها؟"
- "إذا كنت سأفكر في السفر إلى اليابان لهذا العلاج، ما السجلات والاختبارات الطبية التي سأحتاج إلى تحضيرها؟"
كيف يمكن لـ CancerCareE المساعدة
في CancerCareE، نحن متخصصون في تنسيق الوصول إلى العلاجات المتقدمة للسرطان في جميع أنحاء العالم. بينما العلاج الضوئي المناعي معتمد حالياً فقط في اليابان، يمكننا:
- مساعدتك في فهم ما إذا كنت قد تكون مرشحاً محتملاً بناءً على سجلاتك الطبية
- ربطك بمستشفيات شريكة في اليابان تجري هذا الإجراء
- تنسيق عملية السفر الطبي بالكامل بما في ذلك المساعدة في التأشيرة، مواعيد المستشفى، خدمات الترجمة، والإقامة
- تقديم دعم مستمر طوال رحلة علاجك
ملاحظة مهمة: نحن لا نقدم العلاج الطبي بأنفسنا. نحن ننسق الوصول إلى المستشفيات المعتمدة ومقدمي الخدمات الطبية. جميع القرارات الطبية يتخذها أطباء مرخصون في المؤسسات الشريكة.
مستعد لاستكشاف خياراتك؟
أرسل سجلاتك الطبية لمراجعة أولية من قبل فريق التنسيق لدينا. سنساعدك في فهم ما إذا كان العلاج الضوئي المناعي أو العلاجات المتقدمة الأخرى قد تكون مناسبة لحالتك.
الخلاصة: أمل مع مصداقية
يمثل العلاج الضوئي المناعي تقدماً حقيقياً في علاج سرطان الرأس والرقبة غير القابل للجراحة. للمرضى المختارين بعناية، يقدم:
- معدلات استجابة عالية (75٪ في البيانات الواقعية)
- تمديد ذي معنى في البقاء على قيد الحياة (متوسط البقاء 26.9 شهراً)
- استهداف دقيق مع ضرر ضئيل للأنسجة السليمة المحيطة
- تنشيط مناعي قد يوفر فائدة إضافية طويلة المدى
لكنه ليس علاجاً معجزة للجميع. يتطلب مراكز متخصصة، فرقاً خبيرة متعددة التخصصات، واختياراً دقيقاً للمرضى. البيانات، رغم إثارتها للإعجاب، تأتي من مجموعات صغيرة نسبياً وتحتاج إلى تحقق في تجارب دولية أكبر.
للمريض المناسب، هذه "الجراحة بالضوء من اليابان" هي حرفياً بصيص أمل جديد.
إخلاء مسؤولية: هذه المعلومات لأغراض تعليمية وليست بديلاً عن الاستشارة الطبية المهنية. استشر دائماً مقدم رعاية صحية مؤهل للتشخيص وخيارات العلاج. العلاج الضوئي المناعي باستخدام سيتوكسيماب ساروتالوكان معتمد في اليابان وقد لا يكون متاحاً في بلدان أخرى. التجارب السريرية قد تكون خياراً للمرضى خارج اليابان.
المراجع
- Tahara H, et al. Outcomes of Near-Infrared Photoimmunotherapy for Head and Neck Cancer: A Single-Center Retrospective Study. Cancers. 2026;18(3):350.
- Dynarowicz K, et al. A Decade of Innovation in Breast Cancer (2015-2025): A Comprehensive Review. Cancers. 2026;18(3):361.
- Suzuki S, et al. Predictive Value of EGFR Expression for the Efficacy of Near-Infrared Photoimmunotherapy in Head and Neck Cancer. JMA Journal. 2026.
- Hirakawa H, et al. Preliminary observations on peripheral inflammatory markers in NIR-PIT and ICI-treated recurrent head and neck squamous cell carcinoma. Eur Arch Otorhinolaryngol. 2026.
- Mohiuddin TM, et al. Synthetic zipper mediated pre-targeting system for near-infrared photoimmunotherapy. iScience. 2026.
- Nouso H, et al. Near-infrared Photoimmunotherapy Targeting High-risk Human Neuroblastoma Cells Expressing GD2. Anticancer Res. 2025.
جدول المحتويات
بحاجة لتوجيه خبير؟
منسقونا الطبيون متخصصون في العلاجات المتقدمة للسرطان في اليابان وحول العالم.
أرسل حالتك info@cancercaree.com